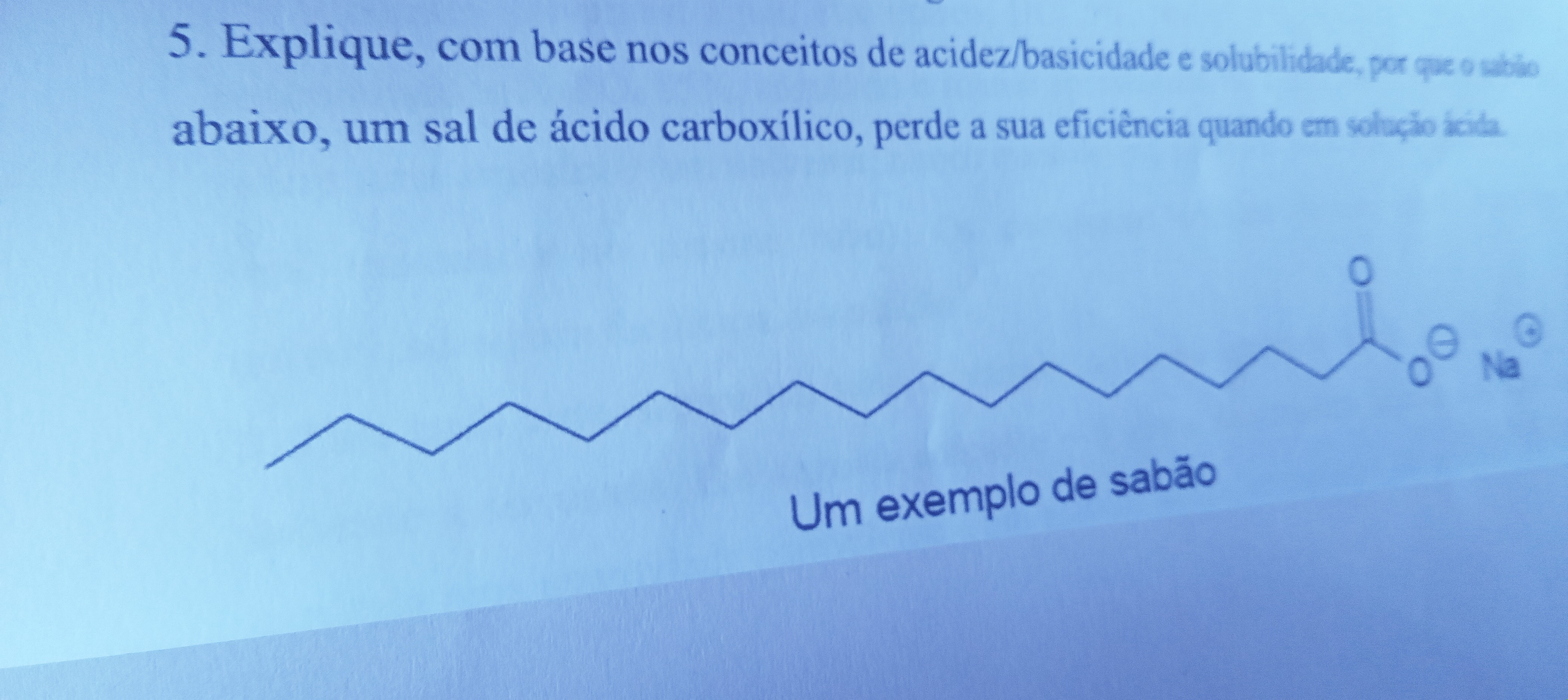
Explique ,com base nos conceitos acidez basicidade e solubilidade porque o sabão abaixo um sal de ácido carboxilico perder solução ácida?
Queria saber essa resposta
💡 1 Resposta
Renan Gonzalez Garcez
O sabão é um sal de ácido carboxílico, e possui propriedades que o tornam solúvel tanto em soluções ácidas quanto em soluções básicas. No entanto, o sabão tende a se tornar menos solúvel em soluções ácidas.
Isso ocorre porque os ácidos tendem a doar íons H+ (íons de hidrogênio) para a solução, tornando-a mais ácida. Quando adicionamos um sabão em solução ácida, esses íons H+ podem interagir com os íons carboxilato presentes no sabão, formando ácido carboxílico, que é menos solúvel em água.
Por outro lado, em soluções básicas, o sabão tende a ser mais solúvel. Isso ocorre porque as bases tendem a aceitar íons H+ da solução, diminuindo a acidez e tornando-a mais básica. Nesse ambiente, o sabão se ioniza em íons carboxilato e íons sódio (ou potássio, dependendo do tipo de sabão), tornando-se mais solúvel em água.
Portanto, a solubilidade do sabão depende tanto da acidez ou basicidade da solução quanto da presença de íons carboxilato. Em soluções ácidas, os íons H+ podem reagir com os íons carboxilato, formando ácido carboxílico e reduzindo a solubilidade do sabão. Em soluções básicas, o sabão se ioniza em íons carboxilato e íons sódio ou potássio, tornando-se mais solúvel.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
porque a maioria dos alcaloides são extraídos de plantas através de uma solução ácida?
Quimica Organica Geral e Experimental
•IFG
Pedro Antonio
Materiais relacionados
 1 pág.
1 pág.





Compartilhar